1. Introdução ao Equilíbrio Químico
O que é Equilíbrio Químico?
O equilíbrio químico é um estado dinâmico que ocorre em reações químicas reversíveis, onde as velocidades das reações direta e inversa se igualam. Neste ponto, as concentrações de reagentes e produtos permanecem constantes ao longo do tempo, embora as reações continuem ocorrendo em ambas as direções.
Importante: O equilíbrio químico é dinâmico, não estático. As moléculas continuam reagindo, mas as velocidades das reações direta e inversa são iguais.
Condições para o Equilíbrio
- Reação Reversível: A reação deve poder ocorrer nos dois sentidos (direta e inversa).
- Sistema Fechado: Especialmente importante para reações com gases, o sistema deve ser fechado para evitar a perda de substâncias.
- Temperatura Constante: O equilíbrio é estabelecido em uma temperatura específica.
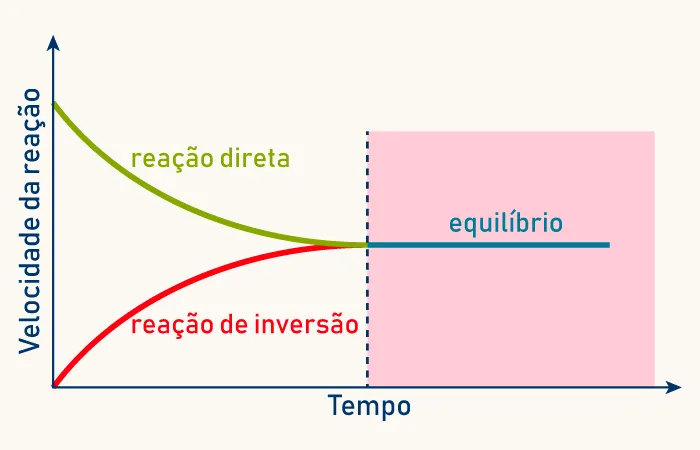
Gráfico mostrando a velocidade da reação direta diminuindo e a velocidade da reação inversa aumentando até se igualarem no equilíbrio.
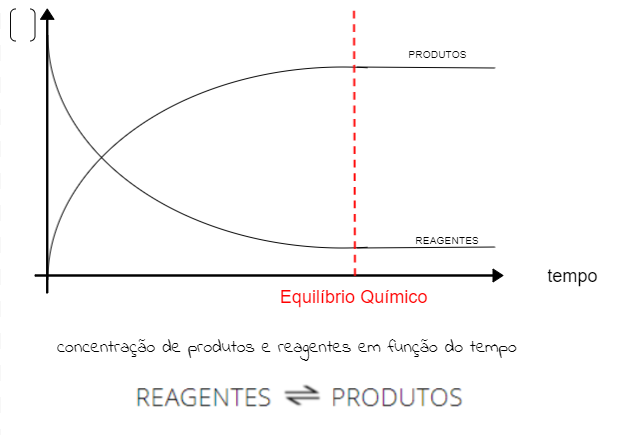
Concentração de produtos e reagentes em função do tempo. No equilíbrio, as concentrações se mantêm constantes.
Representação do Equilíbrio
Uma reação em equilíbrio é representada por uma dupla seta (⇌):
aA + bB ⇌ cC + dD
Onde A e B são reagentes, C e D são produtos, e a, b, c, d são os coeficientes estequiométricos.

Representação visual do equilíbrio dinâmico: as moléculas continuam reagindo em ambas as direções.
2. Tipos de Equilíbrio e Constante de Equilíbrio (Kc)
Tipos de Equilíbrio Químico
Equilíbrio Homogêneo
Todos os participantes da reação (reagentes e produtos) estão na mesma fase física.
Exemplo:
N₂(g) + 3H₂(g) ⇌ 2NH₃(g)
Todos os componentes estão na fase gasosa.
Equilíbrio Heterogêneo
Os participantes da reação estão em fases físicas diferentes.
Exemplo:
CaCO₃(s) ⇌ CaO(s) + CO₂(g)
Sólidos e gás em equilíbrio.
A Constante de Equilíbrio (Kc)
A constante de equilíbrio é uma expressão matemática que relaciona as concentrações de produtos e reagentes no estado de equilíbrio. Para a reação genérica:
aA + bB ⇌ cC + dD
A constante de equilíbrio Kc é expressa como:
Kc = [C]c × [D]d / [A]a × [B]b
Interpretação do valor de Kc:
- Kc >> 1: O equilíbrio favorece os produtos (reação tende a ser completa).
- Kc ≈ 1: Há quantidades significativas de reagentes e produtos no equilíbrio.
- Kc << 1: O equilíbrio favorece os reagentes (reação ocorre pouco).
3. Princípio de Le Chatelier
O que é o Princípio de Le Chatelier?
O Princípio de Le Chatelier afirma que quando um sistema em equilíbrio é perturbado por uma mudança nas condições (concentração, pressão ou temperatura), o sistema reage de modo a minimizar essa perturbação, deslocando o equilíbrio em uma direção que contrabalanceia a mudança.
Ilustração do Princípio de Le Chatelier e os fatores que afetam o equilíbrio.
Fatores que Deslocam o Equilíbrio
1. Concentração
Adição de Reagentes: Desloca o equilíbrio para a direita (formação de produtos).
Adição de Produtos: Desloca o equilíbrio para a esquerda (formação de reagentes).
Remoção de Reagentes: Desloca o equilíbrio para a esquerda.
Remoção de Produtos: Desloca o equilíbrio para a direita.
Exemplo: Na reação N₂ + 3H₂ ⇌ 2NH₃, adicionar mais N₂ ou H₂ favorece a formação de NH₃.
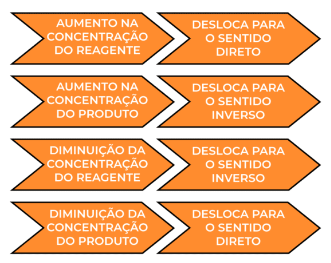
Efeito da variação de concentração no deslocamento do equilíbrio químico.
2. Pressão (para sistemas gasosos)
Aumento da Pressão: Desloca o equilíbrio para o lado com menor número de mols de gás (menor volume).
Diminuição da Pressão: Desloca o equilíbrio para o lado com maior número de mols de gás (maior volume).
Exemplo: Na reação 4P(g) + 6Cl₂(g) ⇌ 4PCl₃(g), aumentar a pressão favorece a formação de PCl₃ (10 mols de gás → 4 mols de gás).
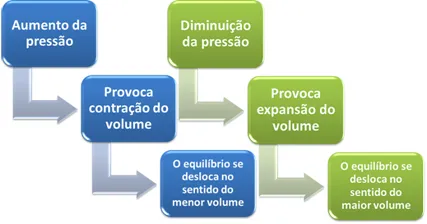
Efeito do aumento e diminuição da pressão no equilíbrio químico.
3. Temperatura
Aumento da Temperatura: Favorece a reação endotérmica (que absorve calor).
Diminuição da Temperatura: Favorece a reação exotérmica (que libera calor).
Exemplo: Na reação N₂ + 3H₂ ⇌ 2NH₃ + calor (exotérmica), aumentar a temperatura favorece a decomposição de NH₃ (reação inversa).
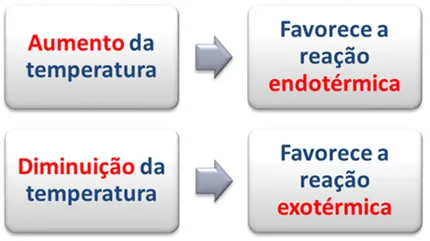
Efeito da temperatura em reações exotérmicas e endotérmicas no equilíbrio químico.
4. Catalisadores
Os catalisadores aumentam a velocidade tanto da reação direta quanto da inversa na mesma proporção, fazendo com que o equilíbrio seja atingido mais rapidamente.
Importante: Catalisadores NÃO deslocam o equilíbrio e NÃO alteram o valor de Kc. Eles apenas aceleram o processo de alcançar o equilíbrio.
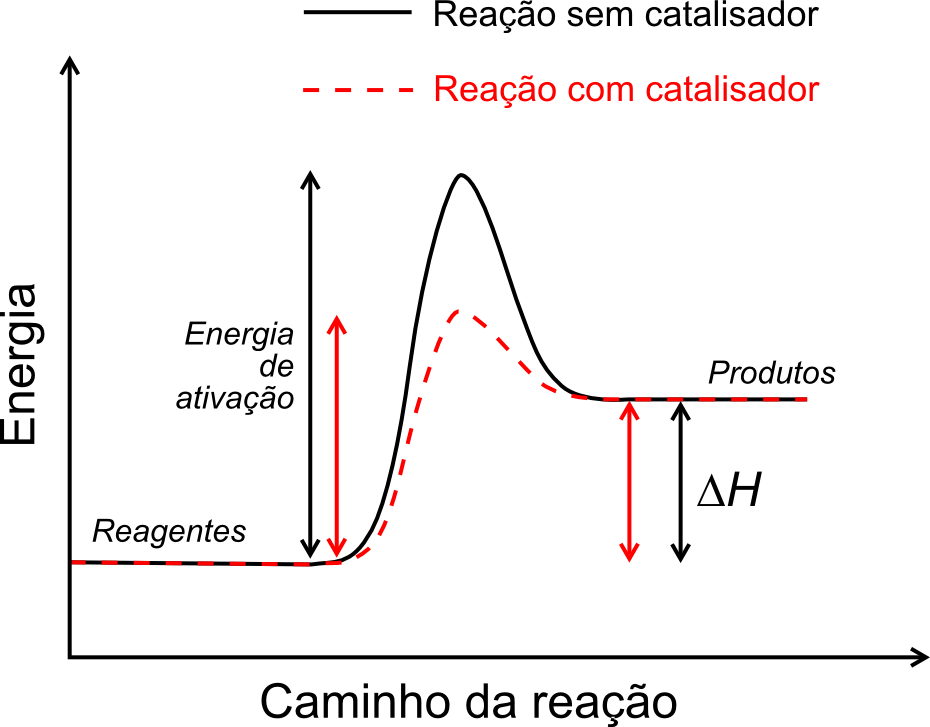
Gráfico mostrando como o catalisador reduz a energia de ativação sem alterar o equilíbrio.
4. Equilíbrio Iônico: Acidez e Basicidade
Autoionização da Água
A água pura sofre um processo de autoionização, onde moléculas de água reagem entre si formando íons hidrônio (H₃O⁺ ou simplesmente H⁺) e íons hidróxido (OH⁻):
H₂O(l) ⇌ H⁺(aq) + OH⁻(aq)
ou, de forma mais completa:
2H₂O(l) ⇌ H₃O⁺(aq) + OH⁻(aq)
Produto Iônico da Água (Kw)
O produto iônico da água (Kw) é a constante de equilíbrio para a autoionização da água. A 25°C, seu valor é:
Kw = [H⁺] × [OH⁻] = 1,0 × 10⁻¹⁴
Interpretação:
- Solução Neutra: [H⁺] = [OH⁻] = 1,0 × 10⁻⁷ mol/L
- Solução Ácida: [H⁺] > [OH⁻] → [H⁺] > 1,0 × 10⁻⁷ mol/L
- Solução Básica: [H⁺] < [OH⁻] → [H⁺] < 1,0 × 10⁻⁷ mol/L
pH e pOH
Para facilitar o trabalho com concentrações muito pequenas de íons H⁺ e OH⁻, utilizamos escalas logarítmicas:
pH = -log[H⁺]
pOH = -log[OH⁻]
A relação entre pH e pOH é dada por:
pH + pOH = 14
Escala de pH:
- pH < 7: Solução ácida
- pH = 7: Solução neutra
- pH > 7: Solução básica
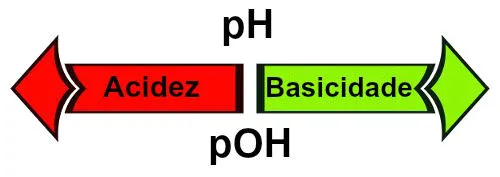
Relação entre pH e pOH: acidez e basicidade.
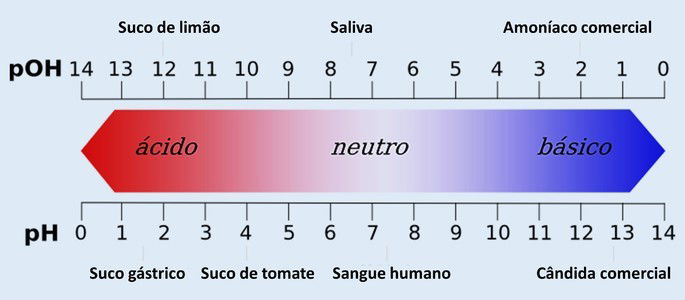
Escala de pH com exemplos de substâncias comuns.
Constantes de Acidez (Ka) e Basicidade (Kb)
As constantes Ka e Kb são medidas quantitativas da força de ácidos e bases em solução aquosa.
Constante de Acidez (Ka)
Para um ácido genérico HA que se dissocia em água:
HA(aq) ⇌ H⁺(aq) + A⁻(aq)
Ka = [H⁺][A⁻] / [HA]
Quanto maior o Ka, mais forte é o ácido.
Constante de Basicidade (Kb)
Para uma base genérica BOH que se dissocia em água:
BOH(aq) ⇌ B⁺(aq) + OH⁻(aq)
Kb = [B⁺] × [OH⁻] / [BOH]
Quanto maior o Kb, mais forte é a base.
Relação entre Ka, Kb e Kw
Para um par ácido-base conjugado, existe uma relação importante entre suas constantes:
Ka × Kb = Kw = 1,0 × 10⁻¹⁴
Importante: Quanto mais forte for um ácido (Ka alto), mais fraca será sua base conjugada (Kb baixo), e vice-versa.
5. Hidrólise Salina
O que é Hidrólise Salina?
A hidrólise salina é a reação entre os íons de um sal e a água, que pode alterar o pH da solução. É essencialmente o processo inverso da neutralização ácido-base.
Sal + Água ⇌ Ácido + Base
Quando um sal é dissolvido em água, seus íons podem reagir com as moléculas de água, dependendo da força do ácido e da base que originaram o sal.
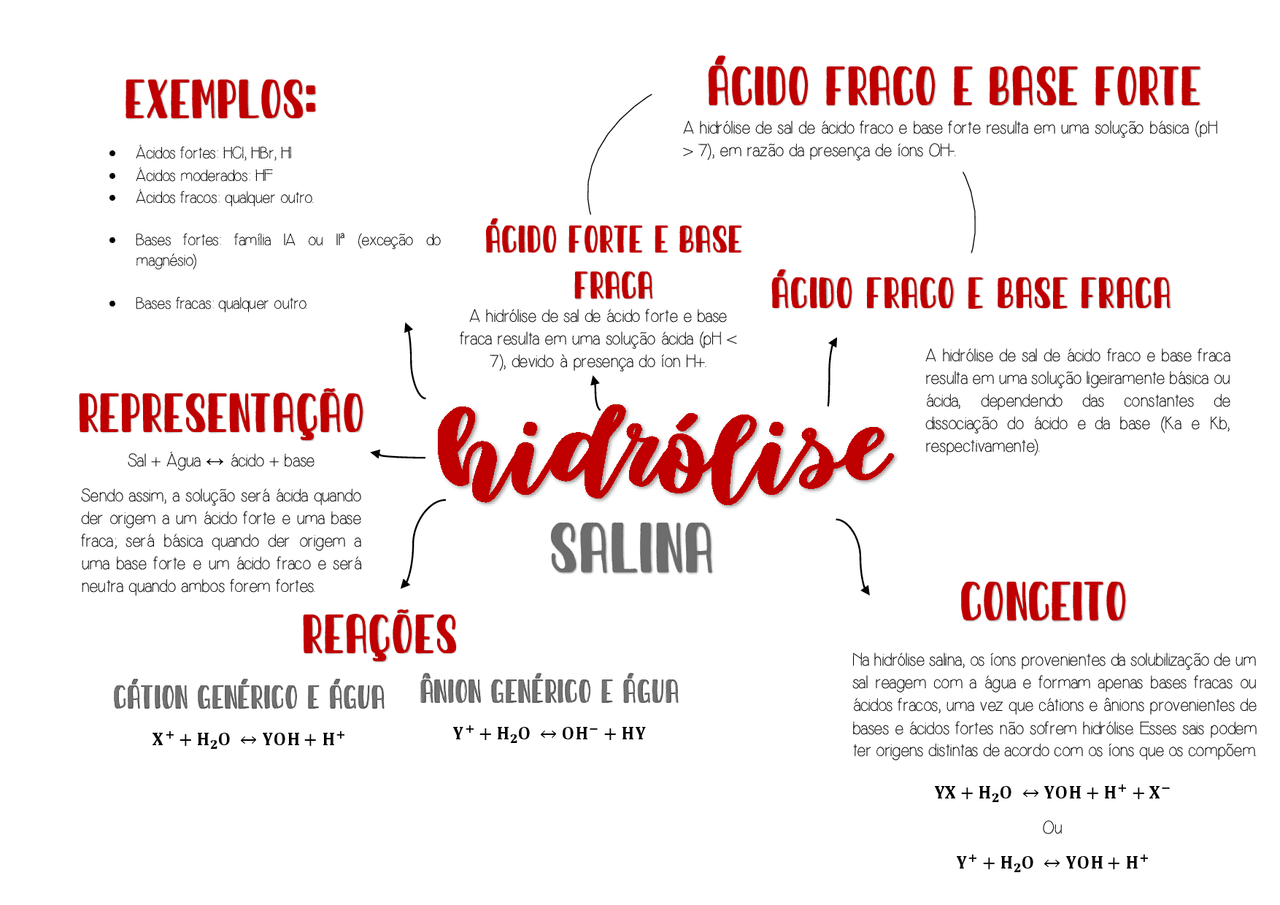
Resumo completo sobre hidrólise salina, incluindo tipos e exemplos.
Tipos de Hidrólise Salina
1. Sal de Ácido Forte e Base Forte
Não ocorre hidrólise. Os íons do sal não reagem com a água.
Exemplo: NaCl (cloreto de sódio)
NaCl → Na⁺ + Cl⁻
Na⁺ vem de NaOH (base forte) e Cl⁻ vem de HCl (ácido forte). Nenhum dos íons reage significativamente com a água.
2. Sal de Ácido Forte e Base Fraca
Hidrólise do cátion. O cátion proveniente da base fraca reage com a água, liberando H⁺.
Exemplo: NH₄Cl (cloreto de amônio)
NH₄⁺ + H₂O ⇌ NH₃ + H₃O⁺
O íon NH₄⁺ (da base fraca NH₃) sofre hidrólise, tornando a solução ácida.
3. Sal de Ácido Fraco e Base Forte
Hidrólise do ânion. O ânion proveniente do ácido fraco reage com a água, liberando OH⁻.
Exemplo: NaCH₃COO (acetato de sódio)
CH₃COO⁻ + H₂O ⇌ CH₃COOH + OH⁻
O íon CH₃COO⁻ (do ácido fraco CH₃COOH) sofre hidrólise, tornando a solução básica.
4. Sal de Ácido Fraco e Base Fraca
Hidrólise de ambos os íons. O pH depende dos valores de Ka e Kb.
Exemplo: NH₄CH₃COO (acetato de amônio)
Ambos os íons sofrem hidrólise. Se Ka > Kb, a solução será ácida; se Kb > Ka, será básica; se Ka ≈ Kb, será aproximadamente neutra.
Constante de Hidrólise (Kh)
A constante de hidrólise (Kh) mede a extensão da hidrólise e está relacionada com Kw, Ka e Kb:
Para hidrólise de cátion:
Kh = Kw / Kb
Para hidrólise de ânion:
Kh = Kw / Ka
6. Solução Tampão (Efeito Tampão)
O que é uma Solução Tampão?
Uma solução tampão (ou solução tamponada) é uma solução que resiste a grandes variações de pH quando pequenas quantidades de ácidos ou bases são adicionadas. Essas soluções são fundamentais em processos biológicos e industriais onde o controle de pH é crítico.
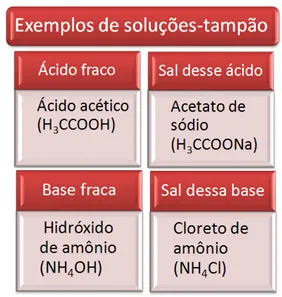
Exemplos de soluções-tampão: ácido fraco com sal de ácido e base fraca com sal de base.
Composição de uma Solução Tampão
Uma solução tampão é geralmente formada por:
Tampão Ácido
Ácido fraco + Sal de sua base conjugada
Exemplo:
CH₃COOH (ácido acético) + CH₃COONa (acetato de sódio)
Tampão Básico
Base fraca + Sal de seu ácido conjugado
Exemplo:
NH₃ (amônia) + NH₄Cl (cloreto de amônio)
Como Funciona o Efeito Tampão?
O sistema tampão funciona através do equilíbrio entre o ácido/base fraco e seu par conjugado:
Para um tampão ácido (HA/A⁻):
HA(aq) ⇌ H⁺(aq) + A⁻(aq)
Adição de ácido (H⁺):
O íon A⁻ (base conjugada) reage com o H⁺ adicionado:
A⁻ + H⁺ → HA
Neutraliza o ácido adicionado, minimizando a variação de pH.
Adição de base (OH⁻):
O ácido fraco HA reage com o OH⁻ adicionado:
HA + OH⁻ → A⁻ + H₂O
Neutraliza a base adicionada, minimizando a variação de pH.
Equação de Henderson-Hasselbalch
O pH de uma solução tampão pode ser calculado pela equação de Henderson-Hasselbalch:
pH = pKa + log([A⁻]/[HA])
Onde pKa = -log(Ka) é o logaritmo negativo da constante de acidez do ácido fraco.
Importante: Um tampão é mais eficaz quando [A⁻] ≈ [HA], ou seja, quando pH ≈ pKa.
Exemplo Biológico: Tampão Bicarbonato no Sangue
O sistema tampão mais importante no corpo humano é o tampão bicarbonato, que mantém o pH do sangue entre 7,35 e 7,45:
H₂CO₃(aq) ⇌ H⁺(aq) + HCO₃⁻(aq)
Este sistema é vital para a manutenção do pH sanguíneo. Variações significativas podem levar a condições graves como acidose (pH < 7,35) ou alcalose (pH > 7,45).

Resumo completo sobre soluções tampão e titulação.
7. Produto de Solubilidade (Kps)
O que é o Produto de Solubilidade?
O produto de solubilidade (Kps) é a constante de equilíbrio para a dissolução de um composto iônico pouco solúvel em água. Ele representa o equilíbrio entre o sólido não dissolvido e seus íons em solução saturada.
Para um sal genérico AxBy que se dissocia:
AxBy(s) ⇌ xA+(aq) + yB-(aq)
Kps = [A⁺]x × [B⁻]y
Importante: O sólido não aparece na expressão do Kps, pois sua concentração é constante.
Interpretação do Kps
- Kps alto: O composto é mais solúvel em água.
- Kps baixo: O composto é pouco solúvel em água (praticamente insolúvel).
Exemplos de valores de Kps (a 25°C):
- AgCl: Kps = 1,8 × 10⁻¹⁰ (pouco solúvel)
- BaSO₄: Kps = 1,1 × 10⁻¹⁰ (pouco solúvel)
- CaCO₃: Kps = 3,4 × 10⁻⁹ (pouco solúvel)
- PbI₂: Kps = 7,1 × 10⁻⁹ (pouco solúvel)
Previsão de Precipitação
O produto iônico (Q) é calculado da mesma forma que o Kps, mas usando as concentrações atuais dos íons (não necessariamente em equilíbrio). Comparando Q com Kps, podemos prever se haverá formação de precipitado:
Q < Kps
A solução pode dissolver mais soluto. Não há precipitação.
Q = Kps
A solução está em equilíbrio. Não há precipitação nem dissolução.
Q > Kps
Há excesso de íons. Ocorre precipitação até que Q = Kps.
Exemplo Prático
Problema:
Ao misturar soluções de AgNO₃ e NaCl, haverá formação de precipitado de AgCl?
Dados: [Ag⁺] = 1,0 × 10⁻⁴ mol/L e [Cl⁻] = 1,0 × 10⁻⁵ mol/L
Kps(AgCl) = 1,8 × 10⁻¹⁰
Solução:
Calcular o produto iônico Q:
Q = [Ag⁺] × [Cl⁻] = (1,0 × 10⁻⁴) × (1,0 × 10⁻⁵) = 1,0 × 10⁻⁹
Como Q (1,0 × 10⁻⁹) > Kps (1,8 × 10⁻¹⁰), haverá formação de precipitado de AgCl.
Efeito do Íon Comum
A presença de um íon comum (um íon que já faz parte do equilíbrio) diminui a solubilidade de um sal. Isso ocorre porque, de acordo com o Princípio de Le Chatelier, o equilíbrio se desloca no sentido de consumir o íon adicionado, favorecendo a formação do precipitado.
Exemplo: A solubilidade de AgCl em água pura é maior do que em uma solução que já contém íons Cl⁻ (como NaCl).
